尚未在境内上市的国际创新药械通过“港澳药械通”引入内地的通道已成熟,至今已惠及6700多人。但药占比、耗占比等考核或许会影响公立医院的“放开使用”。
撰文丨文 慧
通讯员丨彭福祥、梁嘉韵、姚瑞逸
责编丨崔佳慧
Rh阴性血型妈妈又被称为“熊猫血”妈妈,再次生育时面临着胎儿或新生儿溶血的高度风险。
最有效的预防措施是在适当的时候注射抗D免疫球蛋白。但是,抗D免疫球蛋白并未在内地上市,境内“熊猫血”妈妈们要么奔波于港澳求药,要么没能在需要时间内完成注射,孕期一直不能安心。
如今,香港大学深圳医院(简称港大深圳医院)、中山大学附属第一医院(简称中山一院)通过“港澳医械通”引进了抗D免疫球蛋白,她们在深圳、广州就能得到安全有保障的注射,且价格比自购更有优势。

“熊猫血”妈妈的留言。图:中山一院官微截图
这些创新药品器械的引进,为患者带来了实实在在的福利。通过“港澳药械通”政策,无法得到有效治疗的罕见病患者、治疗遇到瓶颈急需新突破的患者能获得国际最新的药物治疗和手术治疗方案。
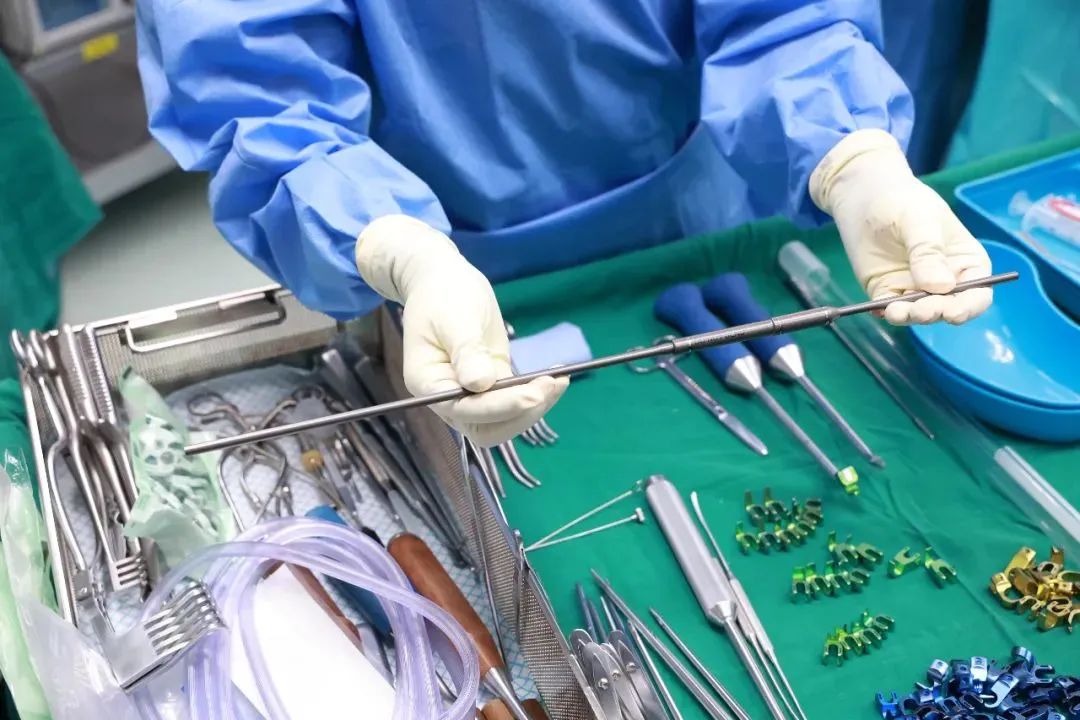
磁力可控延长钛棒。图:港大深圳医院。
截至2024年6月21日,运行3年多的“港澳药械通”政策已经引入63个国际先进创新药品器械,并应用于内地临床,惠及患者6709人次,为患者的医疗需求提供了新的可能。
“港澳药械通”是指已在港澳上市的药品,以及港澳公立医院已采购使用、具有临床应用先进性的医疗器械,可在大湾区内地9市指定医疗机构使用。
已纳入大湾区19家内地医院
审批最快仅需1天
2020年11月,市场监管总局、国家药监局等部门联合印发《粤港澳大湾区药品医疗器械监管创新发展工作方案》。此监管创新举措被称为“港澳药械通”政策。2021年1月-7月,试点工作在港大深圳医院进行。
作为从零开始的参与者,港大深圳医院设备科高级经理赵晖感受到了这三年多时间带来的进展和成效。“试点期是摸着石头过河,一边走,一边形成实践经验,一边完善制度体系建设。如今,全流程都有了制度保障。申报电子化,申请更便捷,审批更快速。”
2021年4月,“港澳药械通”引进的首药、首械在港大深圳医院临床应用,代表着该政策的落地。
2021年8月,广东省药监局联合省卫健委召开专题新闻发布会,宣布“港澳药械通”政策试点结束,在大湾区内地9市正式扩展实施,港大深圳医院等5家医院成为第一批指定医疗机构。
2022年6月,《粤港澳大湾区内地指定医疗机构非首次使用临床急需进口港澳药品医疗器械申报指南》(以下简称《指南》)发布,简化非首次申报材料,申报审批再提速。
2023年10月,《粤港澳大湾区内地指定医疗机构使用临床急需进口药品不良反应/事件报告和监测工作指南(试行)》发布。
至此,从申报到使用到监督,各方面都有了规范。

图:广东省政务服务网
从广东省政府服务网可见,港澳药械通的申请都是在线办理,首次申请的审批日为35个工作日,但药监局承诺办结日为20日。非首次申请审批时限更为快速,根据《指南》,申报已纳入目录的药品医疗器械,申报资料减少至5项,较首次申报而言,非首次申报的申报材料总体减少50%,审批时限平均缩短56%;指定医疗机构申报本机构已获批准的药品医疗器械,申报资料由9项减少至4项,承诺审批时限为1个工作日。
2023年2月,“港澳药械通”扩容至19家医疗机构,纳入多家大型公立三甲医院,包括中山大学附属第一医院、南方医科大学南方医院、广东省人民医院、中山大学孙逸仙纪念医院、广州市第一人民医院南沙医院等。
业内人士认为,这些诊疗量巨大的公立大三甲的加入,无疑会让创新药械的可及性进一步提升。
中山一院于2023年2月加入“港澳药械通”。
药学部主任唐可京介绍,一年多来,医院已经完成近10个新药的引进,涉及肿瘤、高脂血症、偏头痛等多个病种,比如针对晚期非小细胞肺癌KRAS G12C突变的靶向药物索妥拉西布和治疗小细胞肺癌的药物芦比替定,因为国内尚无同类药物上市,故将极大满足这部分患者的临床用药需求。
她表示,从提出申请到落地应用的各环节目前都已较为清晰流畅。首次申请的最快的仅用了3个月;非首次申请的则更为简便,如其他医院曾用过,不用答辩只用函评即可;若是本医院曾引进过的药品“续单”,审批更可谓飞速。
2023年,中山一院引入了一款新型的人工耳蜗,用于一位鼻咽癌放疗后的极重度感音神经性聋患者。医学工程部主任余冬兰介绍,医院于6月30日递交申请材料至省药监局,8月2日就获得了批件,对于新产品而言,这是非常快的。
什么样的创新药械
能够走“港澳药械通”?
截至今年6月,广东省药监局已发布了六批粤港澳大湾区内地临床急需进口港澳药品医疗器械目录,累计批准临床急需进口港澳药品医疗器械63个。
广东省药监局行政许可处副处长梁云指出,在评审阶段,药监局主要针对三个方面,安全有效性、指定医疗机构内部使用及管理的制度及最重要的临床急需性。有些医院在答辩的时候对此把握不准,会导致难以获批。
港大深圳医院是应用最多的医疗机构,迄今,已引入22个创新药品11个创新器械。赵晖认为,港大深圳医院的成功经验便是院内前期遴选精准。“临床需求报上来之后,在初审调研阶段就严格按照《规定》要求进行筛选,必须满足这些条件。”
• 国内没有注册上市
• 港澳已上市,器械已在港澳公立医院使用
• 具有临床先进性
• 同时考量相应企业有一定合作意向,能密切配合
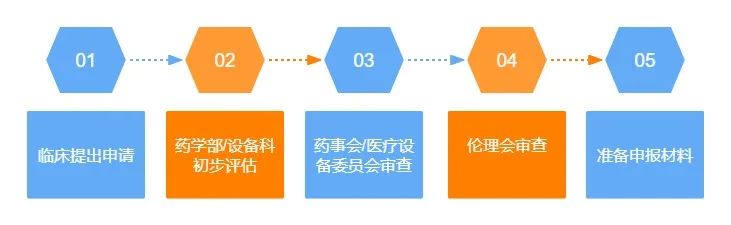
港大深圳医院院内申请流程
中山一院药学部副主任唐欲博表示,医院内部初审时特别看重创新性,要求能够填补临床空白,或者具有不可替代的独特靶点。
如何保证“港澳药械通”
产品临床使用安全?
在药监局的审查中,医院的内部使用及管理的制度也是重点。《规定》就明确指出,指定医疗机构应当及时分析临床数据,研判控制风险,开展急需药械使用安全性和有效性评价。南都健康联盟、南都民调中心曾就港澳药械通相关话题联合发起网络问卷调查,问及使用进口药械时最优先考虑什么内容,近五成受访者认为安全最重要。
如何保障用药用械安全?香港大学深圳医院已形成了一整套管理机制,首先,创新药械产品必须在医院范围内,由获授权且经过专项培训的医疗团队/专家,严格按照药械说明书的适应症、用法用量等操作,不可超说明书使用;其次,患者必须严格知情同意,要让患者了解药械的情况,对于药械使用可能出现的并发症、疗效与风险都要进行全面告知,严格确保整个药械使用的过程符合临床标准和循证要求,并且满足患者治疗需要,可以真正帮助到患者。如果有副作用或不良事件发生,医院也要做好相应准备,依据临床科室制订的紧急救治预案救治患者。

在使用便利性方面,港大深圳医院则建立了“港澳药械通”专类门诊,患者挂号后,相关医生会帮助患者进入“港澳药械通”就医流程。对于不能面诊但急需临床治疗的患者,还可通过电话随访或远程会诊等方式寻求帮助。医院药房设有专用取药窗口,患者或家属可凭医生处方在“港澳药械通”窗口领取。

“港药通”专用取药窗口。图:港大深圳医院
药占比、耗占比或成束缚
“港澳药械通”实施已经三年多,创新药械快速进入内地的通道已经基本成熟,为患者带来了更多用药用械的选择。但在实际使用中,医院仍未能“放得开”。药占比、耗占比绩效考核或许便是束缚的绳。
2024年2月,广东省医疗保障局印发《关于做好“港澳药械通”医疗服务价格项目有关工作的通知》(下称《通知》),明确提出“港澳药械通”医疗服务价格项目实行省级备案、属地监管,备案“港澳药械通”医疗服务价格项目和价格由指定医疗机构参考境外地区成熟做法,遵循公平、合法和诚实信用的原则自主确定,不以现有项目加收项的形式立项;卫生健康部门确定的指定医疗机构备案后的“港澳药械通”医疗服务价格项目可在本机构中使用,不纳入广东省基本医疗服务和市场调节价服务价格项目目录管理,由医疗机构和患者按自费单独结算。
《通知》解决了“港澳药械通”的收费痛点,但“国考”压力仍在。
根据《国家三级公立医院绩效考核操作手册(2023版)》,三级公立医院药械相关考核指标设置及解释由国家卫生健康委统一研究设定,广东省的政策无法左右“国考”。而创新药械的价格往往较高,药占比、耗占比若因此超标,或会影响“国考”分数等级。
不过,该担忧或能得到解决。广东省市监局日前回函表示,近期,广东省已将相关请示上报国家卫生健康委,就医院使用“港澳药械通”产品影响绩效考核事项专门提出申请,建议对其单独计数,以促进“港澳药械通”产品在高水平公立医院扩大使用,同时吸引更多医疗机构参与“港澳药械通”政策实施。
另外,企业可以更主动地参与进来是医疗机构的普遍期待。赵晖表示,在前期产品信息收集阶段,多数资料需要企业协助提供,如产品的临床使用综述、港澳患者的使用情况及治疗效果、产品技术水平等等,如果企业积极参与,将会明显提高申报效率。唐欲博也表示,在评审阶段,至少要补交两次资料。
“期待有更多创新药械入院,可及性进一步增加,让更多患者受益。”大家不约而同地如是表达对“港澳药械通“的未来期待。



